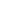多肽化学合成的基本工作原理
发表时间:2026-01-27当前化学合成多肽的方法主要有两种,即Fmoc和tBoc;由于Fmoc比tBoc存在更多优势,所以现在较流行的是Fmoc法。多肽合成是一个重复添加氨基酸的过程,合成方向是从C端(羧基端)向N端(氨基端)进行;过去多肽合成大多是在液相中进行,现在大多采用固相合成,从而大大的降低了每步产品提纯的难度;为了防止副反应的发生,合成柱和添加的氨基酸的侧链都是预先被保护的,只有羧基端是游离的,并且在反应之前必须先用化学试剂活化它。

固相合成路线——以Fmoc合成法为例
具体合成步骤如下:
去保护:Fmoc保护的柱子和单体必须用一种碱性溶剂(piperidine)去除氨基的保护基团。
激活和交联:下一个氨基酸的羧基被一种激活剂所激活溶解,激活的单体与游离的氨基在交联剂的作用下交联,形成肽键。
循环:这两步反应反复循环直到整条肽链合成完毕。
洗脱和脱保护:根据肽链所含的残基不同,用不同的脱树脂溶剂从柱上洗脱下来,其保护基团被一种脱保护剂(TFA)洗脱和脱保护。
多肽是复杂的大分子 , 因此每条序列在物理和化学特性上都是独特的,有些多肽合成很困难 , 另有些多肽虽然合成相对容易 , 但纯化困难;最常见的问题是许多肽不溶于水溶液 , 因此在纯化中 , 这些疏水肽必须溶于非水溶剂中或特殊的缓冲液 , 而这些溶剂或缓冲液很可能不适合应用于生物实验系统 , 因此研究人员不能使用该多肽达到自己的目的 , 因此下面是对于研究人员设计多肽的一些建议。
如何降低肽链合成的难度?
减少序列长度
由于肽的长度增加会导致粗产物纯度降低 , 小于15个残基的肽比较容易得到较高纯度的初产物,当肽链长度增加到20个残基以上时 , 正确产物的量就是一个主要考虑的问题。在许多实验中 , 降低残基数低于20往往能得到更好的实验结果。
减少疏水性残基数
疏水性残基占明显优势的肽,尤其在距C端7-12个残基的区域,常常引起合成困难。这通常被认为是由于合成中形成b折叠片,这样会产生不完全配对。用1个或几个极性残基置换 或加入Gly或Pro以打开肽结构可能会有帮助。
减少“困难”残基
有多个Cys、Met、Arg、Try残基通常难于合成。Ser通常可作为Cys的非氧化替换。
如何增强肽链的可溶性?
改变N端或C端
对于酸性肽 ( 即pH值为7时带负电荷 ), 我们推荐乙酰化 (N端乙酰化 , C端保持自由羧基 ), 以增加负电荷。而对于碱性肽 ( 即pH值为7时带正电荷 ), 我们推荐氨基化 (N端自由氨基 , C端氨基化 ), 以增加正电荷。
缩短或加长序列
某些序列含有大量疏水氨基酸 , 如Trp、Phe、Val、Ile、Leu、Met、Tyr和Ala等 , 当这些疏水残基大于50%通常难于溶解。为了增加肽的极性 , 加长序列可能会有帮助。另外一种选择是通过减少疏水残基的方法降低肽链的长度以增加极性。肽链极性越高 , 就越有可能溶于水。
加入可溶性残基
对于某些肽链而言 , 加上一些极性氨基酸能改善可溶性。我们推荐给酸性肽的 N 端或C端加上Glu-Glu 。给碱性肽的N端或C端加上Lys-Lys 。如果不能加入带电荷基团 , 可以将Ser-Gly-Ser加到N端或C端。但是 , 肽链的两端不能改变时 , 该方法则不可行。
通过置换一个或多个残基改变序列
肽链的可溶性可通过改变序列内某些残基来改善。通常单个残基的替换就能显著改善其疏水性 , 而这种改变通常是较为保守的 , 如用Gly代替Ala。
通过选用不同 “ 框架 ” 来改变序列
如果能用某个序列来制备许多长度一定的相互串连或重叠的多肽 , 则可以用改变各个多肽起始点的方法来实现改变序列的目的。其原理是 : 在同一多肽的亲水和疏水残基间创造新的更好的平衡 , 或将同一多肽内的“ 困难 ”残基 ( 比如2个Cys) 放进两个不同的多肽而不是集于同一分子内。
特殊氨基酸残基对肽链特性影响的一些要点
对于由遗传密码编码的二十种氨基酸及蛋白质中常见的其他氨基酸 , 按其特性可以用几种方法进行分类。目前有最常见的氨基酸的三字母代码和单字母代码,以及不同的分类方法。
免责声明:本文为行业交流学习,版权归原作者所有,如有侵权,可联系删除